(SGGP).- Ngày 23-9, Ủy ban Về các vấn đề xã hội của Quốc hội đã thẩm tra dự án Luật Dược (sửa đổi). Theo Bộ Y tế, dự thảo Luật Dược (sửa đổi) có 14 chương, bổ sung các chương về chính sách của nhà nước về dược và phát triển công nghiệp dược; hành nghề dược; dược lâm sàng và quản lý giá thuốc.
Ngoài ra, dự thảo Luật Dược (sửa đổi) bỏ chương quản lý giá thuốc phải được kiểm soát đặc biệt và đưa các nội dung của chương này vào các phần tương ứng trong dự thảo.
Đáng chú ý, dự thảo Luật Dược (sửa đổi) đã giảm nhiều thủ tục hành chính so với luật hiện hành như: đăng ký thuốc từ 2 năm giảm còn 6 tháng. Đặc biệt, trong dự thảo luật có quy định, dược sĩ có quyền nhắc nhở, yêu cầu các bác sĩ xem xét lại đơn thuốc, đây là quy định nhằm kiểm soát việc kê đơn của các bác sĩ.
Trong dự thảo luật có đề cập đến quy định về nhãn thuốc nhưng chưa có quy định về bao bì dược nên một số ý kiến đại biểu đề nghị cần được bổ sung. Về quản lý giá thuốc, các đại biểu cho rằng, ban soạn thảo cần lưu ý bổ sung quy định cụ thể, tiêu chí thế nào là biến động bất thường. Ông Nguyễn Văn Tiên, Phó Chủ nhiệm Ủy ban Về các vấn đề xã hội của Quốc hội cho rằng, ban soạn thảo nghiên cứu cần có cơ quan quản lý về dược vì trong dự án luật này không thấy nêu cơ quan quản lý.
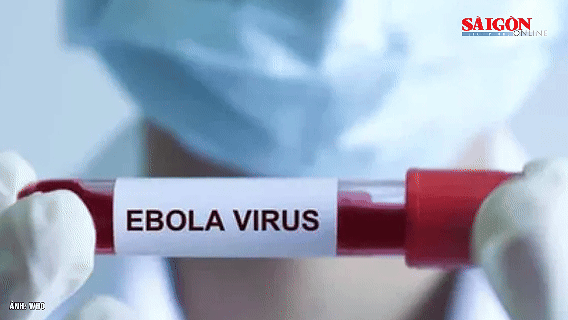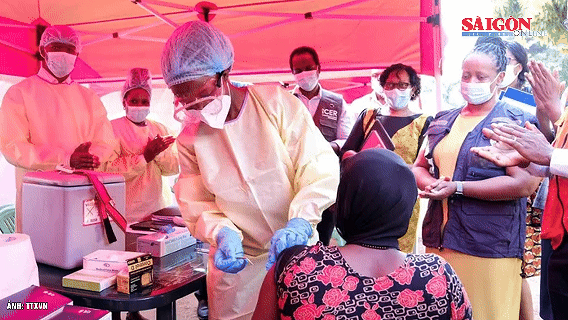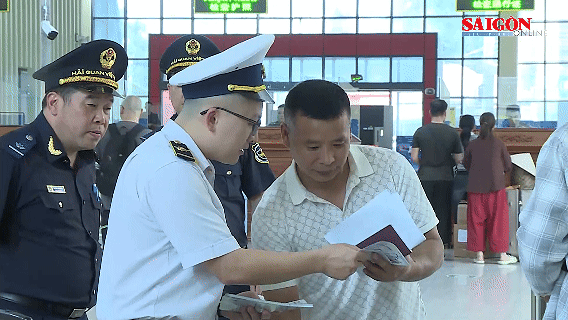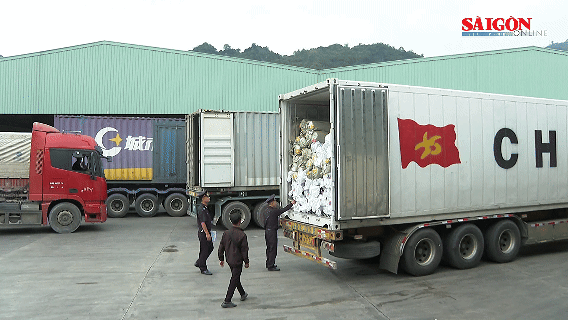
Trong khi đó, trả lời đại biểu về vấn đề kiểm tra thuốc nhập khẩu, ông Nguyễn Tất Đạt, Phó cục trưởng Cục Quản lý dược, Bộ Y tế cho biết, hiện nay trong lĩnh vực dược chúng ta đang hội nhập với Asean và thế giới nên những cam kết công nhận lẫn nhau như: cam kết về thanh tra, kiểm tra… trong các ký kết chúng ta phải thực hiện. Những tổ chức phát triển chúng ta công nhận để nhằm tận dụng tối đa kiến thức của các cơ quan quản lý nước ngoài phát triển, cũng như đáp ứng được thời gian, phù hợp các xu hướng chung. Với những nước chưa tham gia ký kết thì hiện nay phải yêu cầu thanh tra, kiểm tra và thu phí.
MINH KHANG