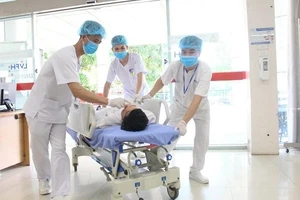
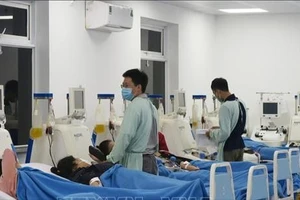
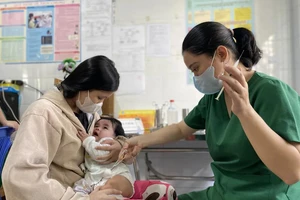
(SGGP). – Ngày 17-12, Bộ trưởng Bộ Y tế Nguyễn Quốc Triệu đã ký quyết định thành lập đoàn thanh tra kiểm tra về việc thực hiện các quy định về công bố lưu hành vaccine Gardasil và Cervarix tại Việt Nam. Đây là 2 loại vaccine phòng chống ung thư cổ tử cung vừa được quyết định cho phép lưu hành cách đây không lâu.
Theo đó, đoàn sẽ thanh tra quá trình nghiên cứu, thẩm định và ban hành quyết định công bố vaccine Gardasil của Công ty Merck Sharp & Dohme (Asia) và vaccine Cervarix của Công ty GlaxoSmithKline. Đồng thời, xem xét và kết luận những tiêu cực (nếu có) trong quá trình công bố cho phép 2 vaccine trên được lưu hành tại Việt Nam.
Bộ trưởng Bộ Y tế cũng quyết định phân công ông Trịnh Quân Huấn, Thứ trưởng Bộ Y tế, làm trưởng đoàn thanh tra trong 15 ngày; đồng thời yêu cầu đoàn báo cáo Ban cán sự, Bộ trưởng Bộ Y tế kết quả thanh tra và kiến nghị xử lý các vi phạm (nếu có) theo quy định của pháp luật.
Được biết, sau khi 2 loại vaccine trên được lưu hành đã có nhiều ý kiến cho rằng, quá trình cấp phép chưa đúng quy trình và việc chỉ định đối tượng tiêm chưa phù hợp. Đáng lưu ý, đã có một số thông tin nghi ngờ rằng, 2 loại vaccine này được cấp phép lưu hành tại Việt Nam là nhờ những cuộc “lobby- vận động hành lang” không trong sạch.
Kh.Nguyễn
Thông tin liên quan |
- Về 2 loại vaccine ngừa ung thư cổ tử cung vừa được lưu hành - “Lobby” để được lưu hành? |